一款創新醫療器械產品獲批上市國家藥品監督管理局經審查,批準了西安康拓醫療技術股份有限公司生產的創新產品“增材制造聚醚醚酮顱骨缺損修復假體”注冊。
該產品基于患者顱骨缺損的影像學數據,創新性采用聚醚醚酮醫用粉料,經選擇性激光燒結增材制造加工而成,能夠匹配患者缺損部位,通過三維嵌入方式實現顱骨缺損替代,恢復患者原顱骨曲率實現缺損區三維重建。
不限 2024 2023 2022 2021 2020 2019 2018 2017 2016 2015 2014 2013 2012 2011 2010 2009 2008 2007 2006

該產品基于患者顱骨缺損的影像學數據,創新性采用聚醚醚酮醫用粉料,經選擇性激光燒結增材制造加工而成,能夠匹配患者缺損部位,通過三維嵌入方式實現顱骨缺損替代,恢復患者原顱骨曲率實現缺損區三維重建。
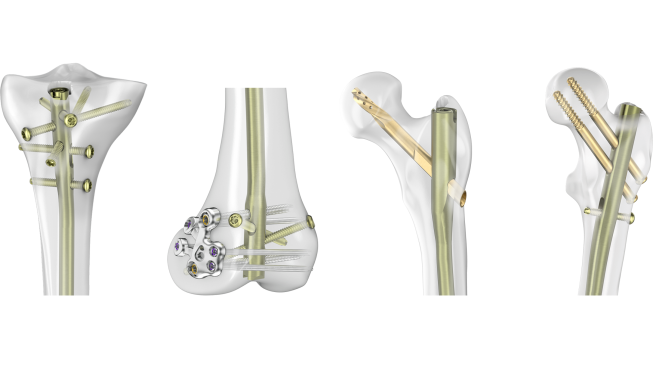
根據WARN法案(The Worker Adjustment and Retraining Notification (WARN) Act,工人調整和再培訓通知法案)要求,公司大規模裁員前需要進行提前公告。強生(J&J)子公司DePuy Spine(隸屬于 DePuy Synthes)在10月30日公布了其在科羅拉多州的Monument工廠將裁員67名員工,以提高公司的盈利能力。

杜塞爾多夫國際醫療器械設備展是綜合性醫療設備展,其規模和影響力居國際同類展會之首。本屆展會吸引來自全球70多個國家和地區的5500多家企業參展,展示醫療器械設備、實驗室分析診斷、電子醫療、醫用耗材、理療矯形共五大細分領域的產品和服務。展會期間還將舉辦200多場各類醫療論壇和講座探討大數據、移動醫療等的應用與發展。
本屆展會上,樂普醫療、安圖生物等1400多家中國企業攜創新產品亮相,向全球醫療市場提供全方位、多樣化的臨床解決方案,成為全球醫療器械行業一支重要的中國力量。

“這是對TekniPlex醫療保健的變革性收購,將我們擴大到醫療技術的合同,開發和制造組織(CDMO)部分,”TekniPlex Healthcare首席執行官Chris Qualters說,“我們有能力通過開發工程材料,共同設計組件和組裝,使用先進的工藝技術和提供無菌屏障產品與我們的全球客戶進行新的醫療技術合作,這使我們能夠與他們真正合作,從概念到護理,以幫助改善患者結果”。
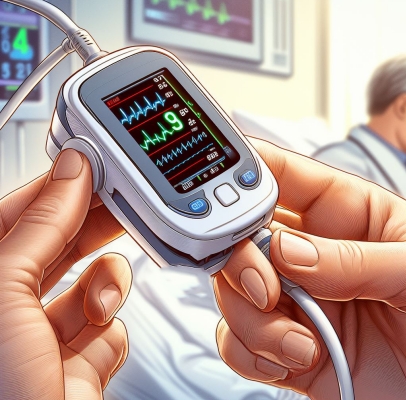
一直以來,人們都擔心脈搏血氧儀(Pulse Oximetry)的準確性會因為膚色差異而出現偏差。當COVID-19大流行期間,脈搏血氧儀被廣泛用于評估病毒對肺部的影響,診斷結果的矛盾出現更加重了這個由來已久的擔心。2021年,FDA開始審視這一問題。

醫療器械PMDA注冊是指在日本厚生勞動省進行醫療器械上市前申請的過程。PMDA是日本厚生勞動省的英文縮寫,負責監管日本的醫療器械市場,對醫療器械的上市前申請進行審批。

醫療器械臨床CRO的首要職責是根據醫療器械的特點和目標,設計科學、嚴謹、可行的臨床試驗方案。試驗方案包括試驗目的、試驗設計、樣本量、觀察指標、數據分析方法等。

創新醫療器械注冊需要提交完整的注冊申請資料,包括產品技術文件、質量管理體系文件、臨床試驗報告等。這些資料必須真實、準確、完整,才能夠通過監管部門的審查。


已有868次查看

已有771次查看
已有789次查看
已有769次查看

已有778次查看

已有881次查看

已有786次查看
已有752次查看
已有771次查看

已有747次查看





