印度(India)醫療器械注冊要點(流程、費用及時間)C、D類產品必須在印度境內進行臨床試驗,除非有認可國家/地區(歐盟、美國、日本、加拿大、澳大利亞)發出的自由銷售證明。
境外生產商首先需要指定印度境內的代理持證人,角色包含總代、注冊代理等,直接與CDSCO溝通注冊等事宜。代理持證公司具體收費(代持證書費用、進口業務費用等)自定。代理持證人必須持有有效的批發許可證(表格20B和21B / 21C)。
不限 2024 2023 2022 2021 2020 2019 2018 2017 2016 2015 2014 2013 2012 2011 2010 2009 2008 2007 2006
境外生產商首先需要指定印度境內的代理持證人,角色包含總代、注冊代理等,直接與CDSCO溝通注冊等事宜。代理持證公司具體收費(代持證書費用、進口業務費用等)自定。代理持證人必須持有有效的批發許可證(表格20B和21B / 21C)。

在飛利浦向FDA提交了270份醫療器械報告(Medical Device Reporting,MDR)后,FDA發布了一份安全通訊(原文地址:https://www.fda.gov/medical-devices/safety-communications/carefully-monitor-philips-dreamstation-2-cpap-machines-signs-overheating-fda-safety-communication),警告消費者注意CPAP機器過熱的跡象。這些報告投訴DreamStation 2 CPAP機器存在發熱問題,其中部分報告還詳細說明了患者受傷(例如燒傷)的情況。這270份MDR文件的收集時間從2023年8月1日至2023年11月15日,相比之下,過去三年飛利浦偉康收到的有關該型號器械的MDR還不足30份。

國外TOP 5醫療器械企業2022年收入超50%來自海外,其中西門子收入主要來自德國以外市場;2022年中國TOP 5醫療器械企業除九安醫療外,其他企業產品主要在國內銷售。國內醫療器械企業若想成為全球頭部公司,應將海外市場作為企業重要的發展戰略布局。
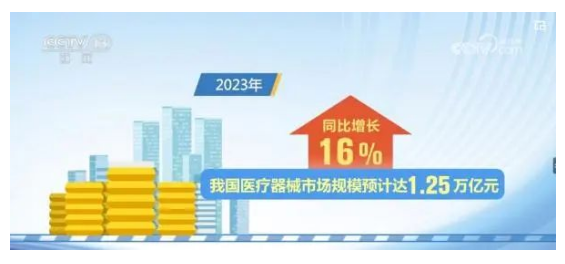
中國物流與采購聯合會11月26日發布2023醫療器械行業發展報告。根據報告,隨著“健康中國”戰略的不斷深化,以及我國人口老齡化和多元化醫療服務需求的不斷增長,我國醫療器械產業持續保持快速發展態勢。
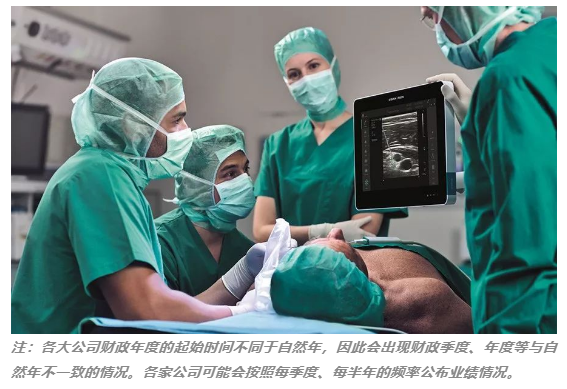
醫療器械以及解決方案供應商邁瑞醫療發布2023年第三季度報告。前三季度公司實現營業收入273.04億元,同比增長17.20%;實現歸母凈利潤98.34億元,同比增長21.38%。第三季度公司實現營業收入88.28億元(約12.35億美元),同比增長11.18%;實現歸母凈利潤33.92億元,同比增長20.52%。

“此次收購將豐富我們的產品組合,特別是其西羅莫司涂層冠狀動脈支架、外周自膨式支架、紫杉醇涂層PTCA和PTA球囊等已獲得CE標志的產品,可望增強我們在PCI和PTA手術中治療病灶的能力。此外,憑借我們強大的銷售網絡,此等高端產品將惠及更多病患者,在推動業務增長的同時,也進一步落實我們致力透過創新技術,改善患者生活質量的承諾。”

FDA計劃重新集中其人員和資源,主要與IMDRF合作。FDA將在2024年主持IMDRF,Shuren在信中邀請徐景和參加明年3月份的IMDRF會議,繼續協調兩個組織之間的討論。

今年以來,健康服務剛性需求逐漸釋放,醫療行業呈現良好的復蘇態勢。隨著“健康中國”戰略的不斷深化,以及我國人口老齡化和多元化醫療服務需求的不斷增長,我國醫療器械產業持續保持快速發展態勢。


已有874次查看

已有775次查看
已有791次查看
已有772次查看

已有781次查看

已有884次查看

已有787次查看
已有755次查看
已有775次查看

已有749次查看





