創新醫療器械注冊會有什么要求和難度?創新醫療器械注冊是一項重要的任務,對于醫療器械的研發者和生產者來說,了解和遵守相關的注冊要求和難度是非常關鍵的。
創新醫療器械注冊需要提交完整的注冊申請資料,包括產品技術文件、質量管理體系文件、臨床試驗報告等。這些資料必須真實、準確、完整,才能夠通過監管部門的審查。
不限 2024 2023 2022 2021 2020 2019 2018 2017 2016 2015 2014 2013 2012 2011 2010 2009 2008 2007 2006

創新醫療器械注冊需要提交完整的注冊申請資料,包括產品技術文件、質量管理體系文件、臨床試驗報告等。這些資料必須真實、準確、完整,才能夠通過監管部門的審查。

外資企業在相當長的時間中幾乎壟斷了內窺鏡市場,產品得到等級醫院的充分認可。不過,近年來國內企業在內窺鏡賽道持續發力,市場份額顯著提升。
該產品由單光子發射計算機斷層掃描系統(SPECT)主機(含兩個SPECT探測器)、CT主機架、檢查床、PDU服務器、采集客戶端工作站、SPECT采集服務器工作站、CT采集重建工作站、影像處理工作站、患者定位監視器、SPECT準直器等組成。
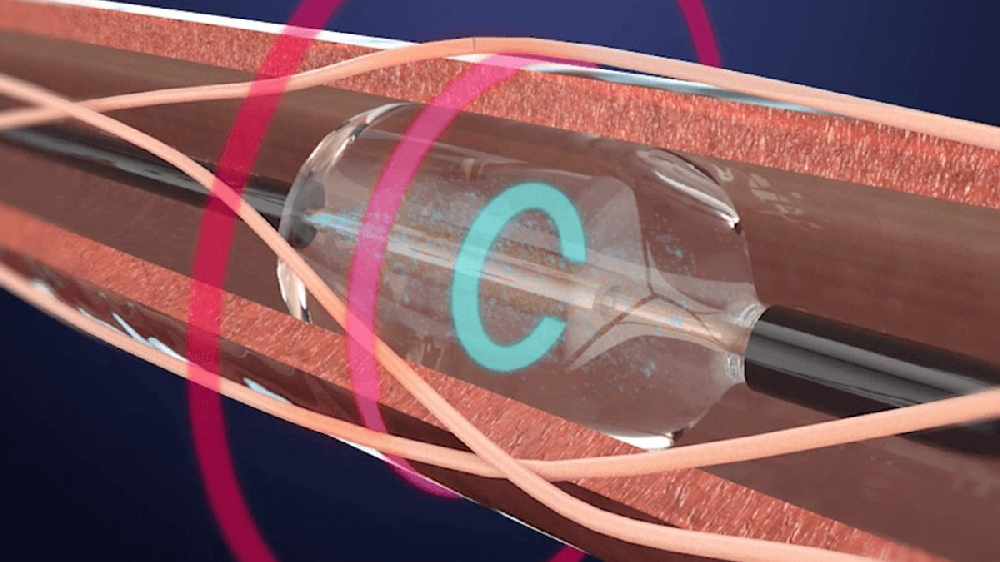
FDA批準的Paradise?系統預期用途聲明該系統適用于生活方式改變和藥物不足以控制血壓的患者。Paradise?系統使用超聲波能量來干擾來自交感神經的信號,其治療機制與美敦力(Medtronic)使用射頻能量的Symplicity Spyral略有不同,Symplicity Spyral已經于2013年獲得了CE。

在會上引發熱烈反響。《報告》深入探討國民健康保健需求與醫療體系改革趨勢,分析線上家庭醫生服務的發展現狀與趨勢,探究家用醫療設備行業的生命周期與未來趨勢,并針對重點場景的需求進行深入研究,展望智能家庭保健醫療的未來價值。

全球領先的骨科產品企業Orthofix在11月6日宣布,將在美國全面商業推廣該公司開發的用于側腰椎椎間融合(Lateral Lumbar Interbody Fusion,LLIF)手術的WaveForm? L側腰椎間系統。

經過激烈角逐,中國醫學科學院阜外醫院主導的“三層結構高分子小口徑人造血管”、天津微納芯科技有限公司主導的“互聯網移動醫療智能生化檢驗系統”、首都醫科大學附屬北京天壇醫院主導的“血管內介入治療機器人的研制及臨床應用研究”、太原理工大學主導的“一種用于下肢動脈閉塞輔助診斷的便攜式踝臂指數測量儀的研發”、中國人民解放軍白求恩國際和平醫院主導的“超聲雙腔微導管在CTO治療中的應用”五個項目獲得北方賽區決賽優勝獎并被推薦參加全國總決賽。


已有868次查看

已有771次查看
已有789次查看
已有769次查看

已有778次查看

已有882次查看

已有786次查看
已有752次查看
已有772次查看

已有747次查看





