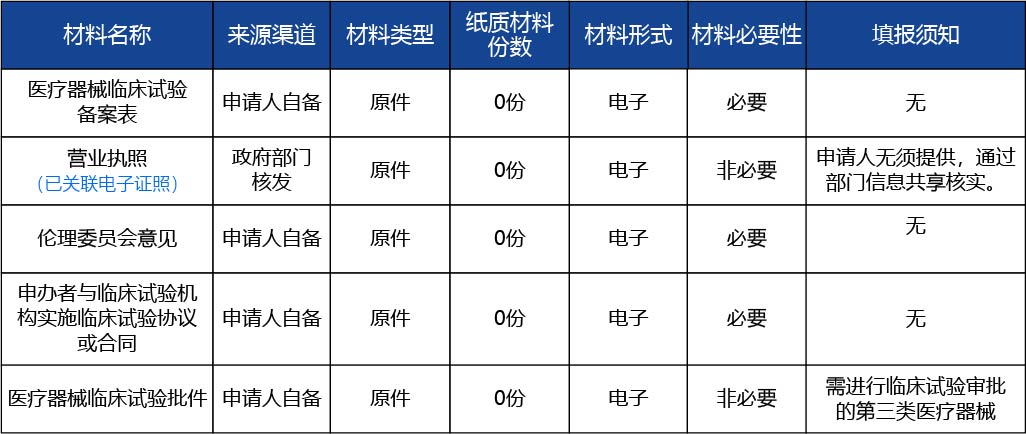
申辦者應(yīng)當(dāng)在試驗(yàn)項(xiàng)目經(jīng)倫理審查通過并與臨床試驗(yàn)機(jī)構(gòu)簽訂協(xié)議或合同。
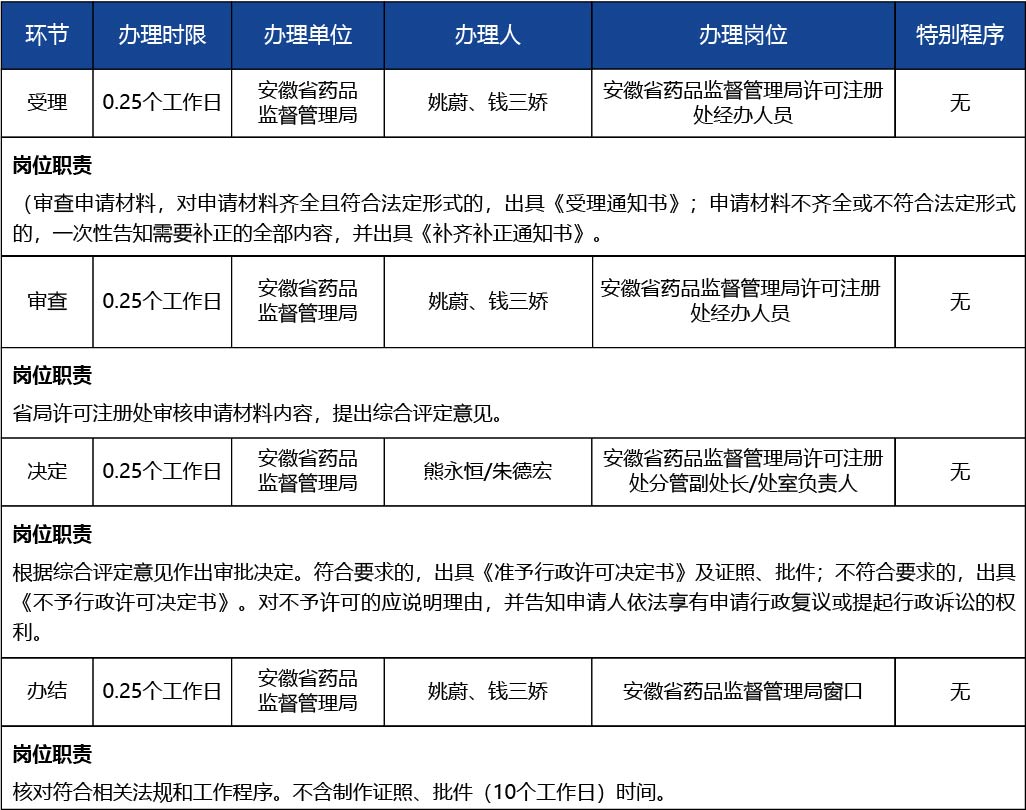
申請人登錄安徽政務(wù)服務(wù)網(wǎng)(https://www.ahzwfw.gov.cn),找到相應(yīng)申請事項(xiàng),提交申報(bào)信息并上傳電子申報(bào)材料。 1.受理:窗口工作人員審查申請材料,對申請材料齊全且符合法定形式的,出具《受理通知書》;申請材料不齊全或不符合法定形式的,一次性告知需要補(bǔ)正的全部內(nèi)容,并出具《補(bǔ)齊補(bǔ)正通知書》。 2.審查:省局許可注冊處審核申請材料內(nèi)容,提出綜合評(píng)定意見。 3.決定:首席代表根據(jù)綜合評(píng)定意見作出審批決定。符合要求的,出具《準(zhǔn)予行政許可決定書》及證照、批件;不符合要求的,出具《不予行政許可決定書》。對不予許可的應(yīng)說明理由,并告知申請人依法享有申請行政復(fù)議或提起行政訴訟的權(quán)利。 4.辦結(jié)送達(dá):根據(jù)申請人申請的送達(dá)方式,省藥品監(jiān)管局窗口送達(dá)《準(zhǔn)予行政許可決定書》及證照、批件或《不予行政許可決定書》,并信息公開。
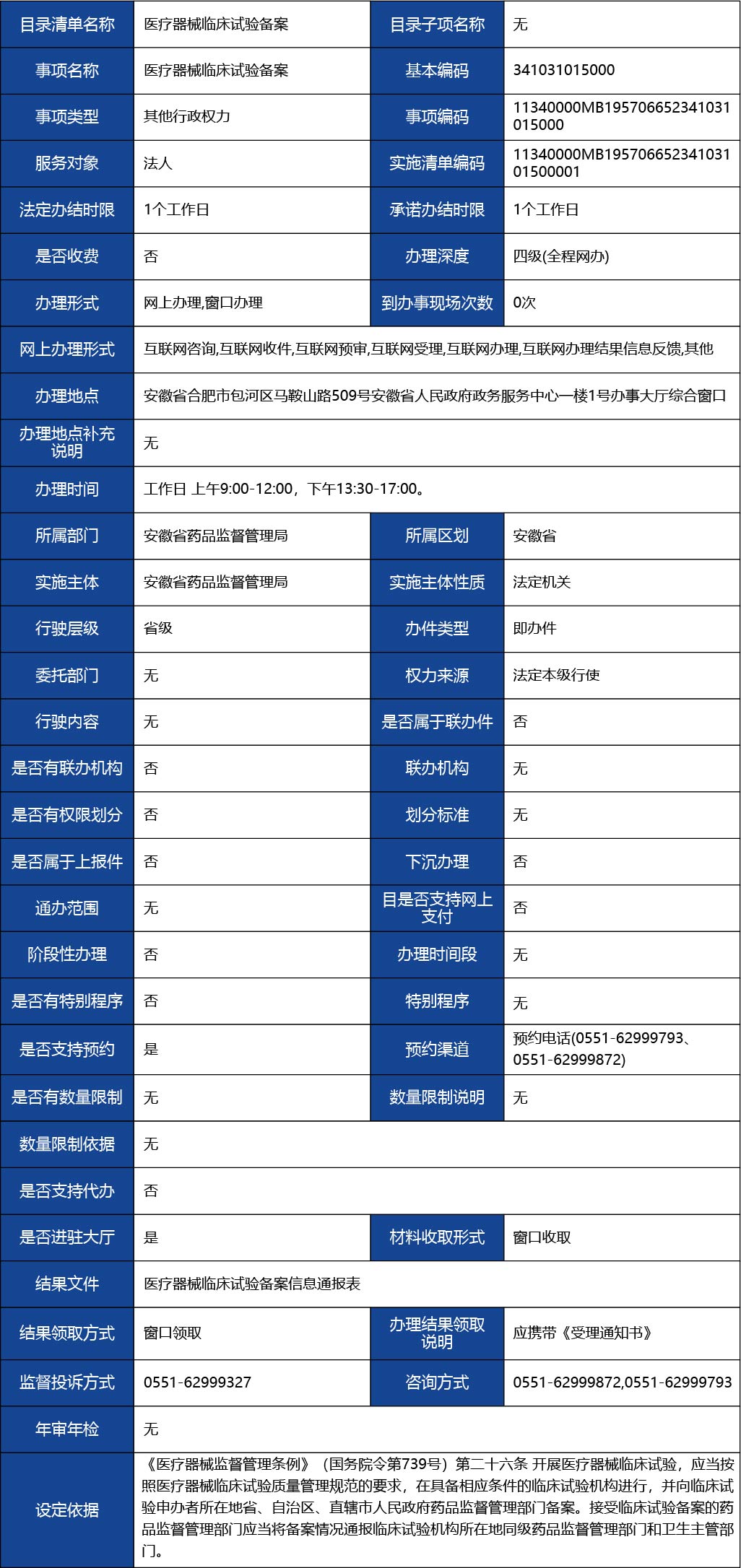
《醫(yī)療器械監(jiān)督管理?xiàng)l例》(國務(wù)院令第739號(hào))第二十六條 開展醫(yī)療器械臨床試驗(yàn),應(yīng)當(dāng)按照醫(yī)療器械臨床試驗(yàn)質(zhì)量管理規(guī)范的要求,在具備相應(yīng)條件的臨床試驗(yàn)機(jī)構(gòu)進(jìn)行,并向臨床試驗(yàn)申辦者所在地省、自治區(qū)、直轄市人民政府藥品監(jiān)督管理部門備案。接受臨床試驗(yàn)備案的藥品監(jiān)督管理部門應(yīng)當(dāng)將備案情況通報(bào)臨床試驗(yàn)機(jī)構(gòu)所在地同級(jí)藥品監(jiān)督管理部門和衛(wèi)生主管部門。
不收費(fèi)

《醫(yī)療器械監(jiān)督管理?xiàng)l例》第十三條 第一款第一類醫(yī)療器···
三類備案人應(yīng)當(dāng)加強(qiáng)醫(yī)療器械全生命周期質(zhì)量管理,對研制、···
二類《醫(yī)療器械監(jiān)督管理?xiàng)l例》第十三條 第一類醫(yī)療器械實(shí)行···
三類《醫(yī)療器械監(jiān)督管理?xiàng)l例》第十三條 第一類醫(yī)療器械實(shí)行···
三類




