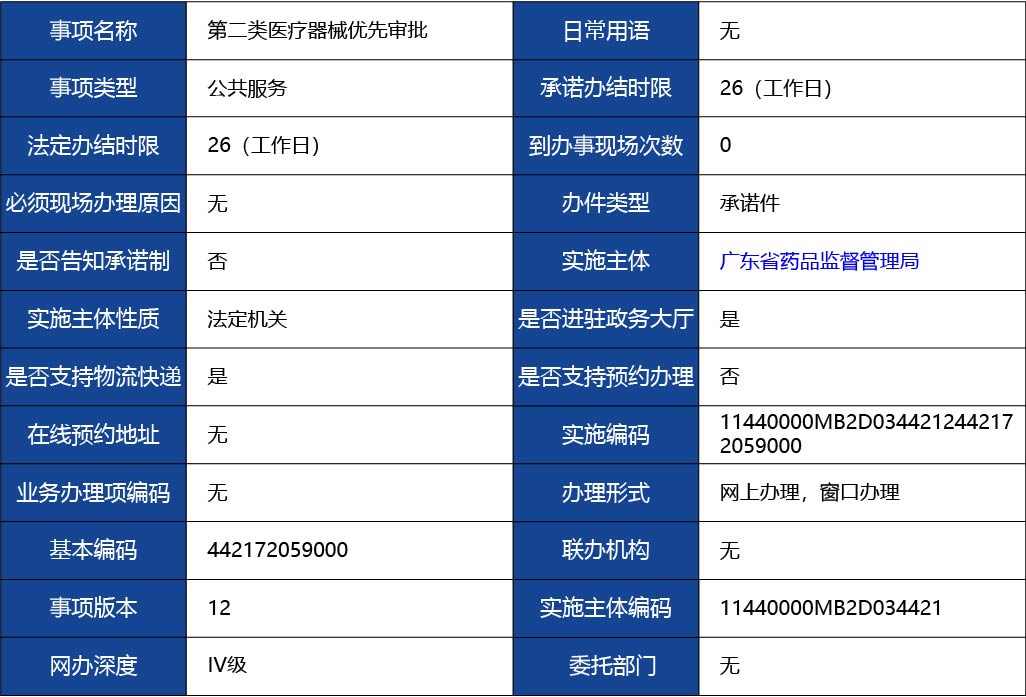
1.企業(yè)注冊地在廣東省內(nèi); 2.符合食藥監(jiān)辦械注〔2015〕511號文中第四條要求,且能提供食藥監(jiān)辦械注〔2015〕511號文中第五條材料的。

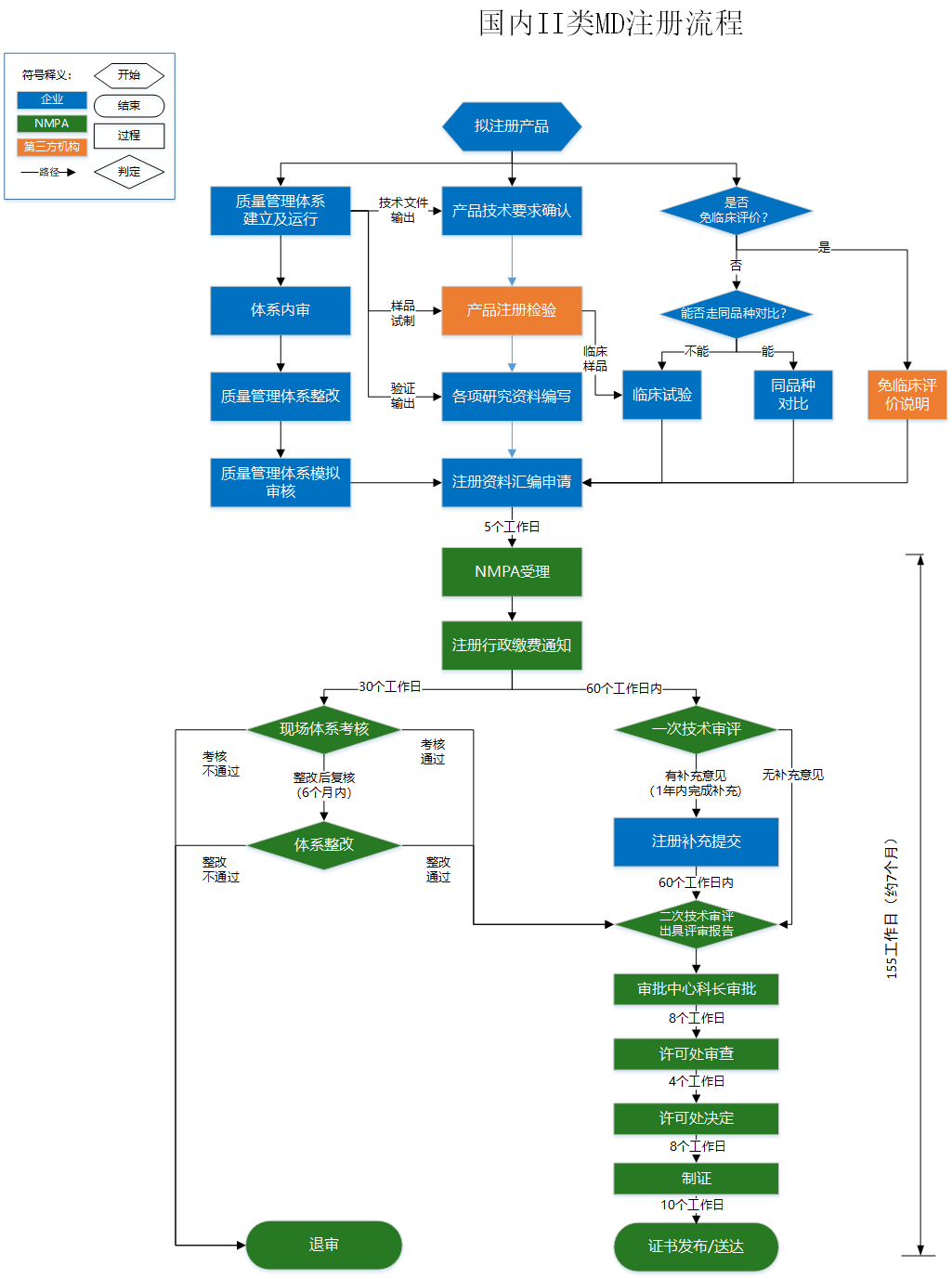
省食品藥品監(jiān)督管理局對同時(shí)符合下列情形的醫(yī)療器械按本程序?qū)嵤┨貏e審批: (一)申報(bào)產(chǎn)品為第二類醫(yī)療器械,申請人屬于我省轄區(qū),申報(bào)產(chǎn)品擬由申請人生產(chǎn)。 (二)申報(bào)產(chǎn)品擁有如下知識(shí)產(chǎn)權(quán)或獲獎(jiǎng)證明之一: 1.國家級發(fā)明獎(jiǎng)、科技進(jìn)步獎(jiǎng); 2.省級科技進(jìn)步獎(jiǎng)二等獎(jiǎng)以上; 3.市級科技進(jìn)步獎(jiǎng)一等獎(jiǎng); 4.核心技術(shù)發(fā)明專利; 5.實(shí)用新型專利(與臨床應(yīng)用相關(guān))。 (三)申報(bào)產(chǎn)品具有顯著的臨床應(yīng)用價(jià)值,產(chǎn)品技術(shù)為國內(nèi)領(lǐng)先,或可填補(bǔ)省內(nèi)該品種醫(yī)療器械的空白,或可替代同類進(jìn)口產(chǎn)品。 (四)申請人已完成申報(bào)產(chǎn)品的前期研究并具有基本定型產(chǎn)品,研究過程真實(shí)和受控,研究數(shù)據(jù)完整和可溯源。
不收費(fèi)(廣東省藥監(jiān)局)
《醫(yī)療器械監(jiān)督管理?xiàng)l例》第十三條 第一款第一類醫(yī)療器···
三類備案人應(yīng)當(dāng)加強(qiáng)醫(yī)療器械全生命周期質(zhì)量管理,對研制、···
二類《醫(yī)療器械監(jiān)督管理?xiàng)l例》第十三條 第一類醫(yī)療器械實(shí)行···
三類《醫(yī)療器械監(jiān)督管理?xiàng)l例》第十三條 第一類醫(yī)療器械實(shí)行···
三類




