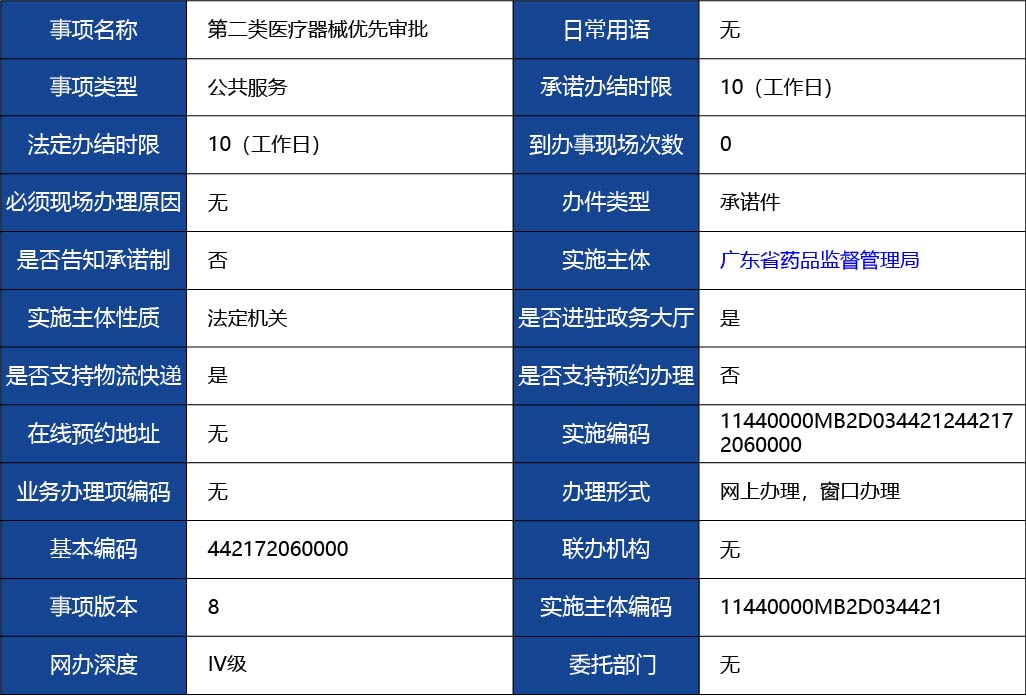
1.企業注冊地在廣東省內; 2.符合粵食藥監局許〔2018〕67號文中第二條要求,且能提供粵食藥監局許〔2018〕67號文中第三條材料的。
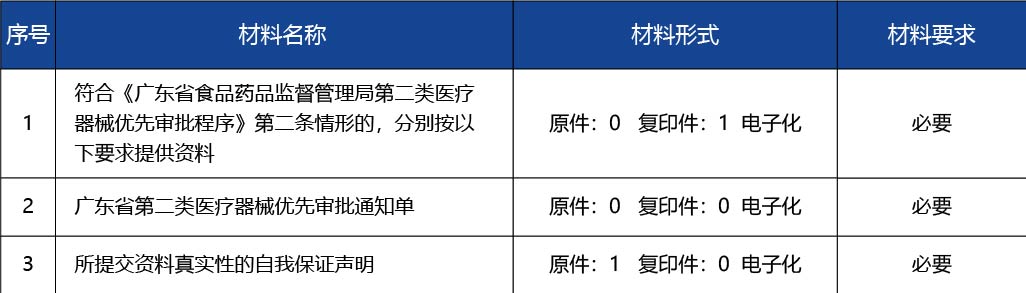
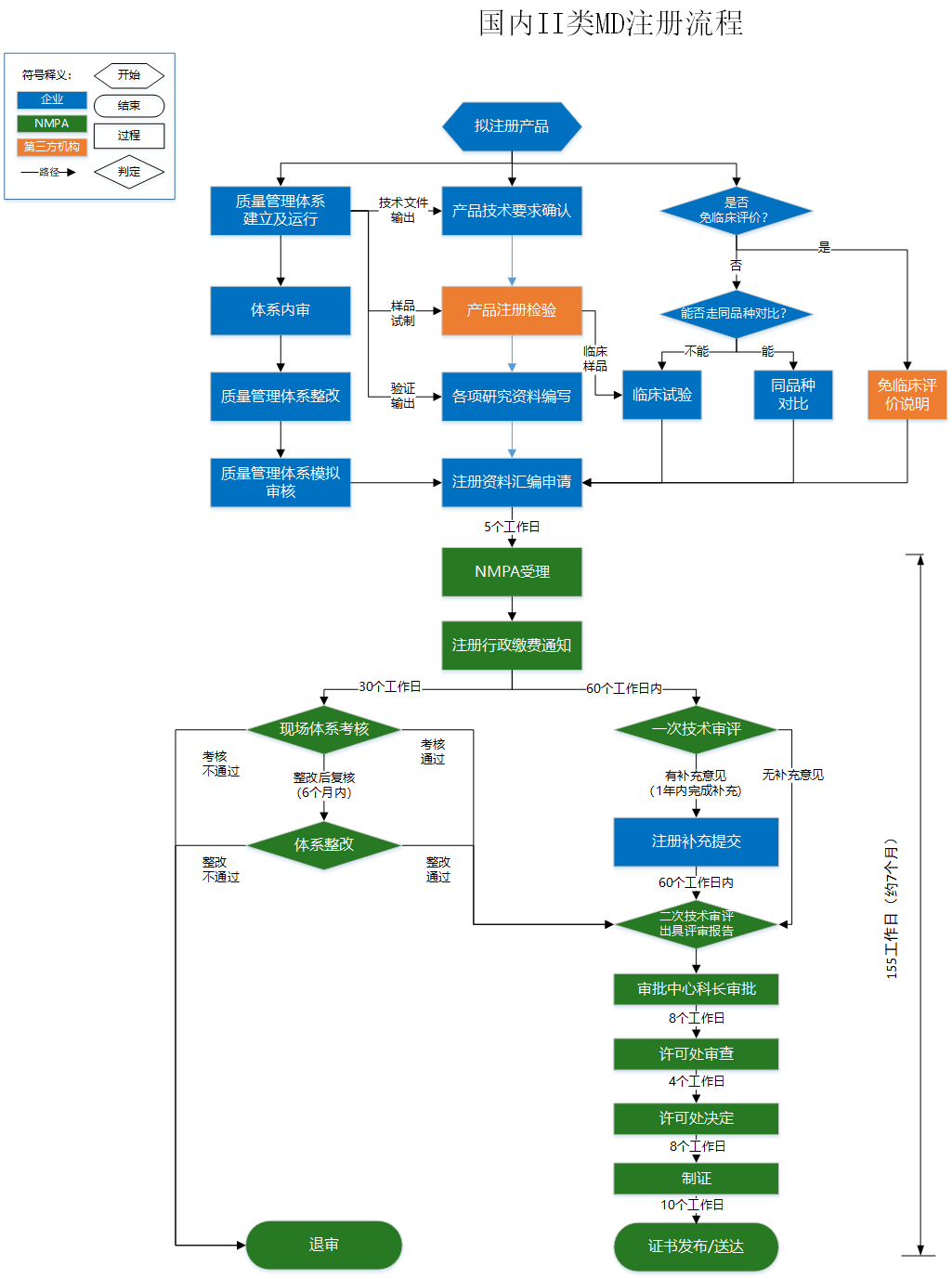
省食品藥品監督管理局(以下簡稱省局)對符合下列情形之一的本省第二類醫療器械首次注冊申請實施優先審批: (一)臨床急需且在本省尚無同品種產品獲準注冊的醫療器械; (二)省內已有同類產品上市,但產品供應不能滿足突發公共衛生事件應急處理需要的醫療器械; (三)診斷或者治療罕見病、惡性腫瘤,且具有明顯臨床優勢的醫療器械; (四)診斷或者治療老年人特有和多發疾病,且目前尚無有效診斷或者治療手段的醫療器械; (五)專用于兒童,且具有明顯臨床優勢的醫療器械; (六)列入國家、廣東省科技重大專項或者國家、廣東省重點研發計劃的醫療器械; (七)廣東省戰略性新興產業骨干企業、廣東省直通車服務重點企業等廣東省重點扶持的醫療器械生產企業申請注冊的醫療器械。
不收費(廣東省藥監局)





